Ösztrogén-kinon indukált DNS változások: A mellrák mechanizmusa?
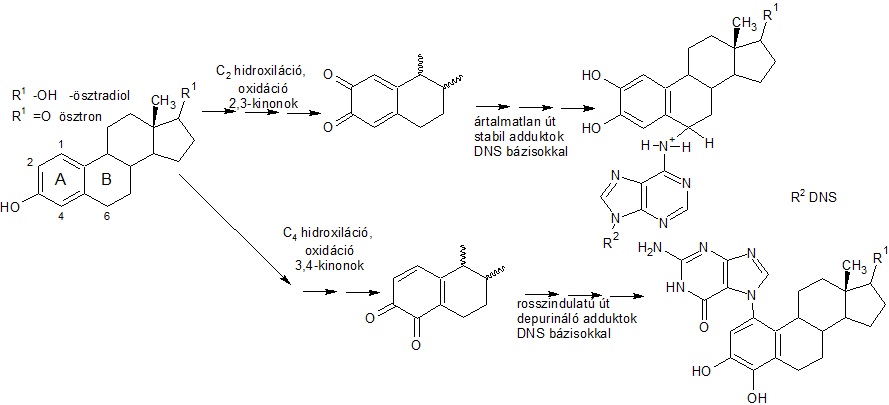
A hosszútávú magas ösztrogén szint, amely akár természetes eredetű, akár hormon helyettesítő terápia következménye, jelentősen megnöveli a mell és petefészek rák kialakulásának valószínűségét [1]. Több elmélet is létezik az ösztrogén rákkeltő mechanizmusának megmagyarázására. Jelen dolgozatban az ösztrogén-kinonok emberi örökítőanyaggal való interakciójára fókuszáltunk. A DNS 2,3-kinonokkal stabil adduktokat képez (melyeket a DNS javító enzimek könnyen kijavítanak), ellenben a 3,4-kinonok hatására kialakuló depurináló adduktok pont mutációkat okozhatnak, és rák kialakulásához vezethetnek hosszabb távon [2].
A munkám célja az, hogy megvizsgáljam a faktorokat, amik befolyásolják az ösztrogén kinonok és DNS purin bázisai közt lejátszódó reakciókat. Ezek között van az ösztrogén molekula B gyűrűjének telítettsége, így megkülönböztethetjük az ösztron, equilin, equilinén molekulákat. Sűrűségfunkcionál elméleten alapuló számítások segítségével tanulmányoztam a 2,3- és és 3,4-ösztrogén-kinonok reakcióját adeninnel és gauninnal. A reakció 3,4-kinon esetén Michael addícióval indul, amely a kinon C1-es szénatomja és az adenin N3-as vagy a guanin N7-es atomja között játszódik le. Ezt követően a kinon gyűrű rearomatizációja történhet meg, proton vesztéssel a C1-es atomon, amit a depurináció követ (ami által megszűnik a C-N kötés a szerves nitrogén bázis és a cukor csoport között), vagy ez a két lépés fordított sorrendben is lejátszódhat.
A 2,3-kinonok sav katalizált tautomerizáció során kinon-metideket alakulnak (kettőskötés alakul ki a C5-C6-os szénatom között). Ezután a kinon-metid C6-os szénatomja elektrofil támadást hajt végre a purin bázis exociklikus amin csoportján, amely stabil adduktot eredményez.
Számításaink során 3 sűrűségfunkcionált (B3LYP, BP86, ωB97xD) használtunk, amelyek eredményeit coupled cluster számításokkal validáltuk. Eredményeink összhangban a kísérleti eredményekkel azt mutatják, hogy a guanin valószínűbb célpontja ezen reakcióknak, mint az adenin. Ezen kívül a B gyűrű telítettsége jelentősen befolyásolja a reakció mechanizmusát.
[1] V. Beral and Million Women Study Collaborators, “Breast cancer and hormone-replacement therapy in the Million Women Study.,” Lancet (London, England), vol. 362, no. 9382, pp. 419–27, 2003.
[2] A. Lábas, B. Krámos, and J. Oláh, “Combined Docking and Quantum Chemical Study on CYP-Mediated Metabolism of Estrogens in Man,” Chem. Res. Toxicol., vol. 30, no. 2, pp. 583–594, 2017.
szerző
-
Girnt Peter
Vegyészmérnöki mesterképzési szak, nappali MSc
mesterképzés (MA/MSc)
konzulens
-
Dr. Oláh Julianna
adjunktus, Szervetlen és Analitikai Kémia Tanszék

