Foszfor-klór kötés hidrolízisének vizsgálata kvantumkémiai módszerekkel
A foszfor-klór kötést tartalmazó vegyületek nagy reakciókészségüknek köszönhetően fontos vegyipari kiindulási anyagok és intermedierek. Ilyen vegyületeket használnak növényvédőszerek (pl. paration, metilparation), egyes gyógyszerek (pl. papaverin) előállításakor. Fontosságukat jelzi, hogy sok reakciókinetikai adatot gyűjtöttek különböző foszforvegyületek hidrolízisének, illetve egyéb nukleofilekkel lejátszódó reakcióinak vizsgálatából. [1] Ugyan kvantumkémiai számítások fontos információkkal tudnának szolgálni a reakciómechanizmusok részleteiről, a fellelt irodalomban nem található utalás arra, hogy a hidrolízis reakciókat vizsgálták volna számításos kémiai eszközökkel is.
TDK munkámban a monoklórfoszfin (PH2Cl) hidrolízisének mechanizmusát vizsgáltam számításos kémiai módszerekkel, a Gaussian09 programcsomag felhasználásával. A reakciókban részt vevő vízmolekulák számát 1 és 5 között változtattam, és vizsgáltam a reakciók aktiválási paramétereit, valamint az átmeneti állapotok szerkezetét a vízmolekulák számának függvényében.
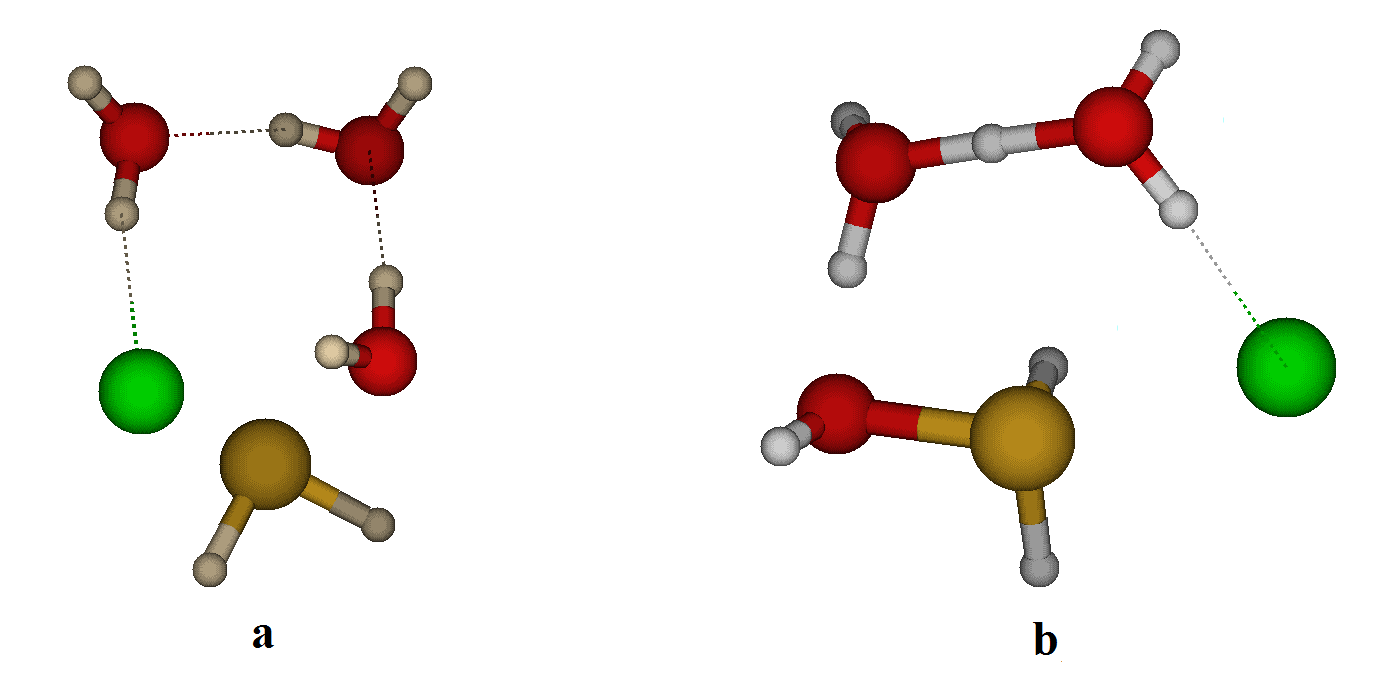
A számítások alapján a hidrolízis alapvetően kétféle úton mehet végbe. Az egyik esetben (a) a vízmolekula a klóratommal megegyező térfélben, a klóratom mellett támad a foszforatomon. Ez a reakcióút egy tetragonális piramis alakú átmeneti állapoton keresztül megy végbe, és ha a vegyület királis lenne, akkor a konfiguráció retenciójával járna. A másik esetben (b) a vízmolekula a klóratommal ellentétes oldalról közelíti meg a foszforatomot. Ez egy trigonális bipiramis alakú átmeneti állapoton keresztül játszódik le, és a konfiguráció inverziójával jár. Egyik talált reakcióút esetén sem találtam stabil intermediert, a termék H2POH molekula egy lépésben, egy átmeneti állapoton keresztül lejátszódó reakcióban keletkezik. A korábbi, hasonló molekulákkal elvégzett kísérletek során mindkét átmeneti állapot kialakulását feltételezték, ezek segítségével próbálták magyarázni a különböző kísérleti eredményeket. [2]
Az általam elvégzett számítások szerint a reakció aktiválási energiája, valamint szabadentalpiája a vízmolekulák számának növelésével csökken. 1 vízmolekulával csak retenciós utat találtam. 2 vízmolekula esetén az inverziós reakcióút aktiválási energiája magasabb volt a retenciós útnál. 3 vízmolekula esetén azonban már kissé alacsonyabb volt az inverziós reakcióút aktiválási energiája, ez azonban még mindig túl magas ahhoz, hogy a reakció szobahőmérsékleten lejátszódhasson. A 4 illetve 5 vízmolekulával viszont ezek jelentősen kisebbnek adódtak, mint a retencióval járó reakcióké. Ezen folyamatok aktiválási energiája már lehetővé teheti, hogy a reakciók szobahőmérsékleten is lejátszódhassanak. Ez összhangban van a kísérleti kinetikai mérésekkel, amelyek szerint a foszfor-klór kötést tartalmazó vegyületek és nukleofilek reakciói főként inverzióval játszódnak le. [2] [3]
[1] J. R. Cox, Jr., O. B. Ramsay, Chemical Reviews, 1964, 64, 317-352.
[2] R. J. P. Corriu, J. P. Dutheil, G. F. Lanneau, S. Ould-Kada, Tetrahedron, 1979, 35, 2889-2894.
[3] M. Mikołajczyk, J. Krzywański, Tetrahedron Letters, 1975, 19, 1607-1610.